Ацетилен вода


Для ацетилена (этина) характерны реакции присоединения:
HC≡CH + Cl2 -> СlСН=СНСl
Ацетилен с водой, в присутствии солей ртути и других катализаторов, образует уксусный альдегид (реакция Кучерова). В силу наличия тройной связи, молекула высокоэнергетична и обладает большой удельной теплотой сгорания — 14000 ккал/м³. При сгорании в кислороде температура пламени достигает 3150 °C. Ацетилен может полимеризироваться в бензол и другие органические соединения (полиацетилен, винилацетилен). Для полимеризации в бензол необходим графит и температура в 400 °C.
Кроме того, атомы водорода ацетилена относительно легко отщепляются в виде протонов, то есть он проявляет кислотные свойства. Так ацетилен вытесняет метан из эфирного раствора метилмагнийбромида (образуется содержащий ацетиленид-ион раствор), образует нерастворимые взрывчатые осадки с солями серебра и одновалентной меди.
Ацетилен обесцвечивает бромную воду и раствор перманганата калия.
Основные химические реакции ацетилена (реакции присоединения, сводная таблица 1.):
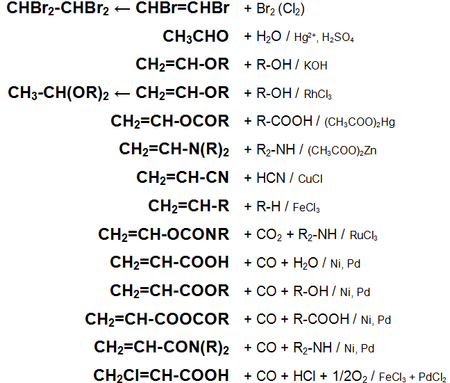
Основные химические реакции ацетилена (реакции присоединения, димеризации, полимеризации, цикломеризации, сводная таблица 2.):
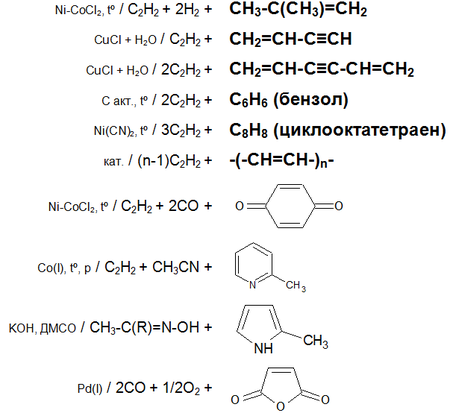
Общие сведения

Ацетилен — ненасыщенный углеводород C 2 H 2 . Имеет тройную связь между атомами углерода, принадлежит к классу алкинов. В природе на Земле практически не встречается, т.к. из-за присутствия кислорода это крайне неустойчивое соединение, получается путем синтеза. Ацетилен обнаружен в атмосфере Урана, Юпитера и Сатурна.
Впервые газообразный ацетилен получил в 1836 г. Эдмунд Дэви при разложении водой карбида калия, полученного при сплавлении металлического калия с углем: К 2 С 2 + 2Н 2 О = С 2 Н 2 + 2КОН.
С конца 19 в., когда был разработан дешевый способ получения ацетилена из карбида кальция (CaC 2 + 2H 2 O = C 2 H 2 + Ca(OH) 2 , который в свою очередь получали прокаливанием смеси угля и негашеной извести (СаО + 3С = СаС 2 + СО), этот газ стали использовать для освещения. В пламени при высокой температуре ацетилен, содержащий 92,3% углерода (это своеобразный химический рекорд), разлагается с образованием твердых частичек углерода, которые могут иметь в своем составе от нескольких до миллионов атомов углерода. Сильно накаливаясь во внутреннем конусе пламени, эти частички обуславливают яркое свечение пламени — от желтого до белого, в зависимости от температуры (чем горячее пламя, тем ближе его цвет к белому). Ацетиленовые горелки давали в 15 раз больше света, чем обычные газовые фонари, которыми освещали улицы. Постепенно они были вытеснены электрическим освещением, но еще долго использовались в небольших фонарях на велосипедах, мотоциклах, в конных экипажах.
Генераторы, в которых для образования ацетилена карбид подаётся в воду, состоят из основной газообразующей камеры и бункера с СаС2. Ёмкость с сухим реагентом находится выше уровня жидкости в резервуаре и когда давление падает ниже определённого значения, происходит вбрасывание новой порции в воду.
В верхней части такой установки имеется газовый отборник, через который газ поступает к сварочной установке либо другим устройствам, работающим на ацетилене. Внизу ёмкости имеется решётка, служащая фильтром для гашённого карбида. Удаление отработанного кальциевого вещества также осуществляется в нижней части генератора через выпускной клапан.
Преимуществом установок работающих по принципу «карбид в воду» является практически полное разложение карбида кальция в воде, хорошее охлаждение и удобство обслуживания и эксплуатации. Недостатком такого вида генераторов ацетилена являются относительно большие размеры и повышенный расход воды. Наиболее часто такие приборы применяются в качестве стационарных газосварочных установок.
Алкины
Алкины — непредельные (ненасыщенные) углеводороды, имеющие в молекуле одну тройную связь С≡С. Каждая такая связь содержит одну сигма-связь (σ-связь) и две пи-связи (π-связи).
Алкины также называют ацетиленовыми углеводородами. Первый член гомологического ряда — этин — CH≡CH (ацетилен). Общая формула их гомологического ряда — CnH2n-2.
Номенклатура и изомерия алкинов
Названия алкинов формируются путем добавления суффикса «ин» к названию алкана с соответствующим числом: этин, пропин, бутин и т.д.
При составлении названия алкина важно учесть, что главная цепь атомов углерода должна обязательно содержать тройную связь. Нумерация атомов углерода в ней начинается с того края, к которому ближе тройная связь. В конце названия указывают атом углерода у которых начинается тройная связь.

Для алкинов характерна изомерия углеродного скелета, положения тройной связи, межклассовая изомерия с алкадиенами.
Пространственная геометрическая изомерия для них невозможна, ввиду того, что каждый атом углерода, прилежащий к тройной связи, соединен только с одним единственным заместителем.
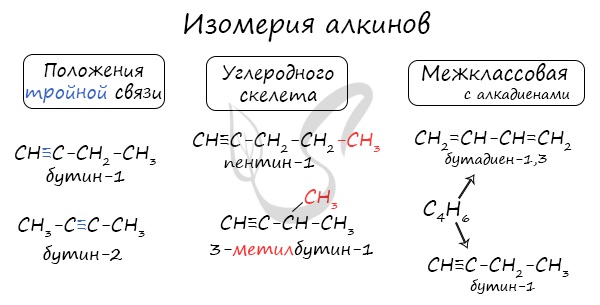
Некоторые данные, касающиеся алкинов, надо выучить:
- В молекулах алкинов присутствуют тройные связи, длина которых составляет 0,121 нм
- Тип гибридизации атомов углерода — sp
- Валентный угол (между химическими связями) составляет 180°
Получение алкинов
Ацетилен получают несколькими способами:
-
Пиролиз метана
При нагревании метана до 1200-1500 °C происходит димеризация молекул метана, в ходе чего отщепляется водород.
Осуществляется напрямую, из простых веществ. Протекает на вольтовой (электрической) дуге, в атмосфере водорода.
2C + H2 → (t, вольтова дуга) CH≡CH
Разложение карбида кальция
В результате разложения карбида кальция образуется ацетилен и гидроксид кальция II.
Получение гомологов ацетилена возможно в реакциях дегидрогалогенирования дигалогеналканов, в которых атомы галогена расположены у одного атома углерода или у двух соседних атомов.

Химические свойства алкины
Алкины — ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны.
Водород присоединяется к атомам углерода, образующим тройную связь. Пи-связи (π-связи) рвутся, остается единичная сигма-связь (σ-связь).
CH≡C-CH3 + H2 → (t, Ni) CH2=CH-CH3 (в реакции участвует 1 моль водорода)
CH≡CH + 2H2 → (t, Ni) CH3-CH3 (в реакции участвует 2 моль водорода)
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу.

Алкины вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена — к наименее гидрированному атому углерода.
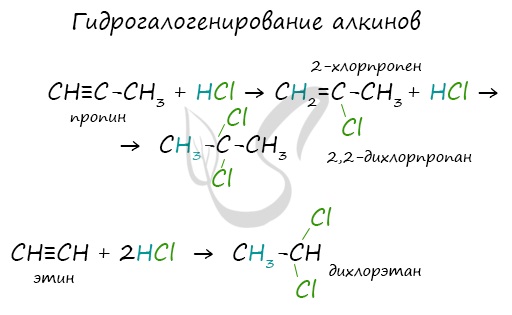
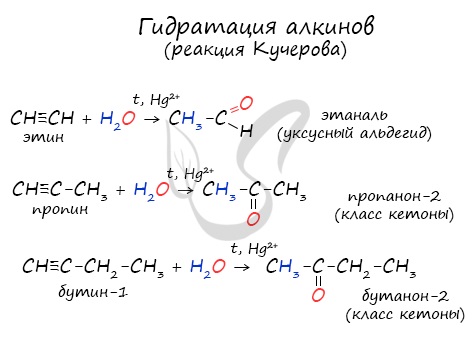
Реакцией Кучерова называют гидратацию ацетиленовых соединений с образованием карбонильных соединений. Открыта русским химиком М.Г. Кучеровым в 1881 году. Катализатор — соли ртути Hg 2+ .
Только в реакции с ацетиленом образуется уксусный альдегид. Во всех остальных реакциях (с гомологами ацетилена) образуются кетоны.
При горении алкины, как и все органические соединения, сгорают с образование углекислого газа и воды — полное окисление.
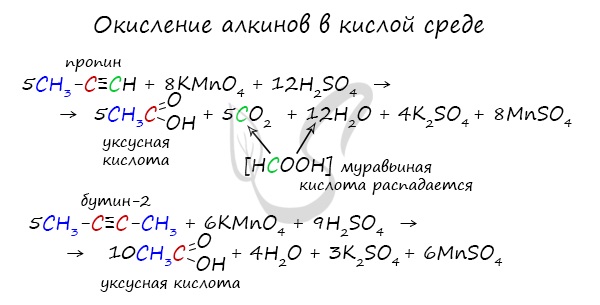
Сильные окислители (особенно в подкисленной среде) способны разрывать молекулы алкинов в самом слабом месте — в месте тройной связи.
Так, при окислении пропина, образуется уксусная кислота и муравьиная кислота, окисляющаяся до угольной кислоты, которая распадается на углекислый газ и воду.
Данная реакция протекает при пропускании ацетилена над активированным углем при t = 400°C. В результате образуется ароматический углеводород — бензол.

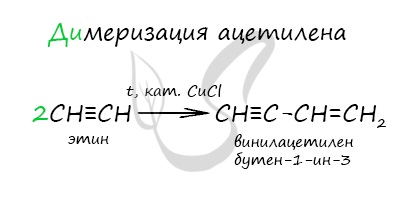
Димеризация ацетилена происходит при наличии катализатора — солей меди I. В результате реакции две молекулы ацетилена соединяются, образуя винилацетилен.
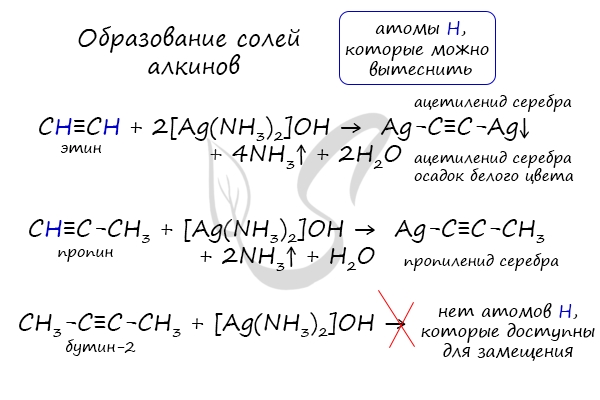
В случае если тройная связь прилежит к краевому атому углерода, то имеющийся у данного атома водород может быть замещен атомом металла. Если тройная связь спрятана внутри молекулы, то образование солей невозможно.
Реакция аммиачного раствора серебра и ацетилена — качественная реакция, в ходе которой выпадает осадок ацетиленида серебра.
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Ацетилен (по ИЮПАК — этин) — непредельный углеводород C2H2. Имеет тройную связь между атомамиуглерода, принадлежит к классу алкинов. При нормальных условиях — бесцветный газ.
Происхождение названия:
Название этого вещества связано со словом «уксус». На латыни acetum – уксус; молекула уксусной кислоты рассматривалась как производное ацетила.


Физические свойства ацетилена:
При нормальных условиях — бесцветный газ, легче воздуха. Чистый 100 % ацетилен не обладает запахом, однако технический ацетилен содержит примеси, которые придают ему резкий запах. Малорастворим в воде, хорошо растворяется в ацетоне. Температура кипения -83,6 °C. Тройная точка -80,55 °C при давлении 961,5 мм рт. ст., критическая точка 35,18 °C при давлении 61,1 атм.
Ацетилен требует большой осторожности при обращении. Может взрываться от удара, при нагреве до 500 °C или при сжатии выше 0,2 МПа при комнатной температуре. Струя ацетилена, выпущенная на открытый воздух, может загореться от малейшей искры, в том числе от разряда статического электричества с пальца руки. Для хранения ацетилена используются специальные баллоны, заполненные пористым материалом, пропитанным ацетоном.
Ацетилен обнаружен на Уране и Нептуне.
Применение ацетилена:
- для газовой сварки и резки металлов,
- как источник очень яркого, белого света в автономных светильниках, где он получается реакцией карбида кальция и воды.
- в производстве взрывчатых веществ.
- для получения уксусной кислоты, этилового спирта, растворителей, пластических масс, каучука, ароматических углеводородов.
- для получения технического углерода
- в атомно-абсорбционной спектрофотометрии при пламенной атомизации
- в ракетных двигателях (вместе с аммиаком).
Безопасность ацетилена:
Поскольку ацетилен не растворим в воде, и его смеси с кислородом могут взрываться в очень широком диапазоне концентраций, его нельзя собирать в газометры.
Ацетилен взрывается при температуре около 500 °C или давлении выше 0,2 МПа; КПВ 2,3—80,7 %, температура самовоспламенения 335 °C. Взрывоопасность уменьшается при разбавлении ацетилена другими газами, например азотом,метаном или пропаном.
При длительном соприкосновении ацетилена с медью и серебром образуются ацетилениды меди и серебра, которые взрываются при ударе или повышении температуры. Поэтому при хранении ацетилена не используются материалы, содержащие медь (например, вентили баллонов).
Ацетилен обладает незначительным токсическим действием. Для ацетилена нормирован ПДКм.р. = ПДК с.с. = 1,5 мг/м? согласно гигиеническим нормативам ГН 2.1.6.1338-03 «Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населённых мест».
ПДКр.з. (рабочей зоны) не установлен (по ГОСТ 5457-75 и ГН 2.2.5.1314-03), так как концентрационные пределы распределения пламени в смеси с воздухом составляет 2,5—100 %.
Хранят и перевозят его в заполненных инертной пористой массой (например, древесным углём) стальных баллонах белого цвета (с красной надписью «А») в виде раствора в ацетоне под давлением 1,5—2,5 МПа.
Свойства ацетилена:
Ацетилен не является особенно токсичным газом, однако это легковоспламеняющийся газ (отсюда его использование при сварке). Основной сложностью при работе с ацетиленом является существенная нестабильность усиливающаяся, когда газ под давлением. Ацетилен может взрываться если давление превышает 200 kPa, а также при приведении к жидкому состоянию, сжатии, нагревании или смешивании с воздухом. В следствии этого при производстве и при работе с ацетиленом необходимо соблюдать специальные меры предосторожности.
Использование ацетилена в баллонах:
Самое распространенное применение ацетилена это исходный материал для различных органических веществ. Второе наиболее часто встречающееся применение ацетилена это горючий компонент при ацетилено-кислородной сварке и резке металла. Коммерчески используемые смеси с ацетиленом включают ацетиленовую сажу, которая используется в батарейках, ацетиленовый спирт применяющийся при производстве витаминов. Так как ацетилен очень взрывоопасен, то его нужно хранить и использовать с особой осторожностью. Когда ацетилен необходимо сжимать под давлением и хранить для ацетилено-кислородной сварки и работ по резке металлов используются специальные баллоны. Баллоны для ацетилена наполнены абсорбирующим материалом и небольшим количеством ацетона. Ацетилен закачивается в баллоны под давлением около 300psi, где он растворяется в ацетоне. В таком состоянии ацетилен теряет возможность взорваться и его безопасно перевозить. Когда вентиль баллона открывают, падение давления приводит к переходу части ацетилена обратно в газообразное состояние, после чего ацетилен по присоединенному шлангу течет до газового резака или сварочной горелки. Ацетилен марки Б может иметь не больше 2% примесей и в основном используется для сварки и резки металлов. Ацетилен марки А может содержать не более 0,5% примесей и больше применяется в процессах химического производства.
Опасность для человека:
Поскольку ацетилен растворим в воде и его смеси с кислородом могут взрываться в очень широком диапазоне концентраций, его нельзя собирать в газометры. Взрывается при температуре около 500 °C или давлении выше 0,2 МПа; КПВ 2,3-80,7 %, температура самовоспламенения 335 °C. Взрывоопасность уменьшается при разбавлении другими газами, например N2, метаном или пропаном. При длительном соприкосновении ацетилена с медью или серебром образуется взрывчатая ацетиленистая медь или ацетиленистое серебро, которые взрываются при ударе или повышении температуры. Поэтому при хранении ацетилена не используются материалы, содержащие медь (например, вентили баллонов). Обладает слабым токсическим действием.
Перевозка:
При заправке, перевозке, хранении и применении Ацетилена необходимо руководствоваться технологической инструкцией, правилами и нормами охраны труда, а также ПБ 03-576-03 «Правилами устройства и безопасной эксплуатации сосудов, работающих под давлением».
Ацетилен в баллонах транспортируются всеми видами транспорта в соответствии с «Правилами перевозки опасных грузов автомобильным транспортом».
Хранят и перевозят его в заполненных инертной пористой массой (например, древесным углем) стальных баллонах белого цвета (с красной надписью «А») в виде раствора в ацетоне под давлением 1,5-2,5 МПа.
Показатели качества ацетилена:
Показатели качества ацетилена растворенного марки «Б» первой категории качества согласно ГОСТ 5457-75
| Наименование показателя | Норма |
| Объемная доля ацетилена, %, не менее | 98,8 |
| Объемная доля воздуха и других малорастворимых в воде газов, %, не более | 1,0 |
| Объемная доля фосфористого водорода, %, не более | 0,05 |
| Объемная доля сероводорода, %, не более | 0,05 |
| Массовая концентрация водяных паров при температуре 20°С и давлении 101,3 кПа (760 мм рт. ст.), г/м2, не более что соответствует температуре насыщения, °С, не выше — 22. | 0,6 |
Вы можете купить Ацетилен в Санкт-Петербурге в магазине Норд Газ по розничной и оптовой цене с доставкой.
Чтобы заказать на сайте Ацетилен, добавьте товар в корзину, или обратитесь к нашим менеджерам по телефонам.
Свойства ацетилена.
Химически чистый ацетилен является бесцветным газом со слабым эфирным запахом и слегка сладковатым вкусом. Технический ацетилен, применяемый для кислородной резки, вследствие присутствия в нем некоторых примесей (сероводорода, аммиака, фосфористого водорода и др.) отличается резким неприятным запахом и является вредным для организма человека.
При давлении свыше 2 кг/см 2 ацетилен в больших объемах приобретает свойства взрывчатого газа и при соприкосновении с накаленной поверхностью или от электрической искры взрывается, при этом температура достигает 3000°С, а давление увеличивается более чем в 10 раз.
С кислородом и воздухом ацетилен образует взрывоопасные смеси, которые от огня взрываются. Ацетилено — воздушная смесь является взрывоопасной при наличии от 2,3 до 81% ацетилена в воздухе. Еще более опасной является ацетилено — кислородная смесь, которая от огня взрывается при содержании в кислороде от 2,3 до 93% ацетилена, при этом скорость распространения взрывной волны достигает 3000 м/сек, поэтому особенно тщательно нужно следить за плотностью всех ацетиленовых приборов, трубопроводов и пр.
Взрывчатость ацетилена сильно понижается при размещении его в капиллярных (очень тонких) каналах. Этим свойством ацетилена пользуются при наполнении баллонов под давлением — ацетиленовые баллоны заполняют специальной пористой массой.
Реакция ацетилена с ацетоном.
Ацетилен хорошо растворяется во многих жидкостях, особенно в ацетоне. В одном объеме ацетона при 15°С и нормальном давлении растворяется 23 объема ацетилена, а при повышенном давлении — пропорционально больше. Это свойство ацетилена также используют при наполнении баллонов. Растворимость ацетилена в ацетоне в значительной степени зависит от температуры: с повышением температуры растворимость уменьшается, а с понижением резко возрастает.
Способность растворенного ацетилена к взрыву понижается.
Реакция сгорания ацетилена.
Ацетилен при сгорании в смеси с чистым кислородом дает пламя с температурой 3050 — 3150°С, а при сгорании в смеси с воздухом 2350°С.
Полное сгорание ацетилена.
Для полного сгорания 1 м 3 ацетилена требуется 2,5 м 3 кислорода или 12,5 м 3 воздуха.
Ацетилен легче кислорода и воздуха. Удельный вес ацетилена при 0°С и 760 мм рт. ст. 1,17 кг/м 3 .
При длительном взаимодействии с красной медью и серебром ацетилен дает соединения, которые при нагревании или при сильном ударе взрываются. Поэтому при изготовлении ацетиленовой аппаратуры и арматуры запрещено применение серебряных припоев и красной меди в чистом виде. Допускаются лишь технические медные сплавы, содержащие не более 70% меди.
Получение ацетилена.
Основным промышленным способом получения ацетилена является разложение карбида кальция водой. Карбид кальция представляет собой химическое соединение кальция с углеродом (СаС2) и является твердым веществом темно-серого или серого цвета.
Технический карбид кальция получается сплавлением негашеной извести с углем (коксом или антрацитом). Шихта, состоящая из смеси угля и извести в определенной пропорции, погружается в электрическую дуговую печь, где под влиянием тепла электрической дуги расплавляется с образованием карбида кальция.
Расплавленный карбид выливают из печи в формы — изложницы, в которых он застывает. Застывший карбид кальция затем дробят, сортируют на куски определенных размеров и упаковывают в специальные барабаны для хранения и транспортировки. Барабаны для упаковки карбида кальция делают из листового железа толщиной не менее 0,5—0,6 мм с герметически закрывающейся крышкой. На цилиндрической поверхности барабанов для повышения их прочности накатаны гофры. Барабан вмещает 50— 130 кг карбида кальция.
Карбидные барабаны следует открывать очень осторожно , так как по тем или иным причинам внутрь барабана может проникнуть влага и образоваться взрывоопасная ацетилено-воздушная смесь. Лучше всего покрыть крышку барабана слоем тавота и снимать ее специальным ножом. Ни в коем случае нельзя прибегать к ударам молотка.
Категорически запрещается при раскупорке карбидных барабанов применять пламя или же вырубать крышку барабана зубилом.
Разложение ацетилена.
При действии воды карбид кальция разлагается, образуя ацетилен и гашеную известь. Реакция протекает по уравнению
и сопровождается значительным выделением тепла.
Карбид кальция при соприкосновении с атмосферным воздухом, содержащим пары воды, разлагается с выделением ацетилена. Из 1 кг карбида кальция обычно получается от 230 до 300 л ацетилена.
Для разложения 1 кг карбида кальция теоретически требуется 0,56 л воды. Реакция разложения карбида протекает с выделением большого количества тепла, поэтому недостаток воды может привести к значительному перегреву и даже воспламенению ацетилена в месте разложения карбида. Во избежание этого процесс разложения карбида ведут всегда с избыточным количеством воды, которая используется для охлаждения. Практически на 1 кг карбида кальция берется от 5 до 20 л воды.
Статья оказалась полезной?! Поделись с друзьями в социальных сетях.
Исходя из тройной связи ацетилена, для него будут характерны реакции присоединения и реакции полимеризации. Атомы водорода в молекуле ацетилена могут замещаться другими атомами или группами. Поэтому можно сказать, что ацетилен проявляет кислотные свойства. Разберем химические свойства ацетилена на конкретных реакциях.
- Гидрирование. Осуществляется при высокой температуре и в присутствии катализатора (Ni, Pt, Pd). На палладиевом катализаторе возможно неполное гидрирование.
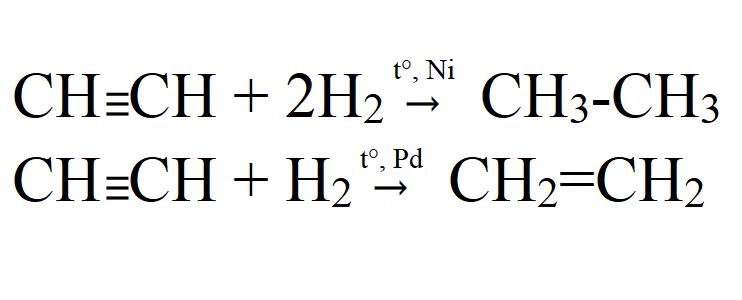
- Галогенирование. Может быть как частичным, так и полным. Идет легко даже без катализаторов или нагревания. На свету хлорирование идет с взрывом. При этом ацетилен полностью распадается до углерода.
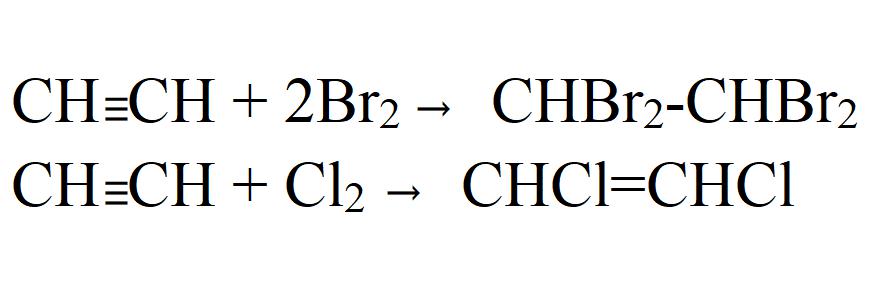
- Присоединение к уксусной кислоте и этиловому спирту. Реакции идут только в присутствии катализаторов.

- Присоединение синильной кислоты.
- Взаимодействие ацетилена с металл-органическими соединениями.
- Взаимодействие с металлическим натрием. Необходима температура 150 °C или предварительное растворение натрия в аммиаке.
2CH≡CH + 2Na → 2CH≡CNa + H2
- Взаимодействие с комплексными солями меди и серебра.
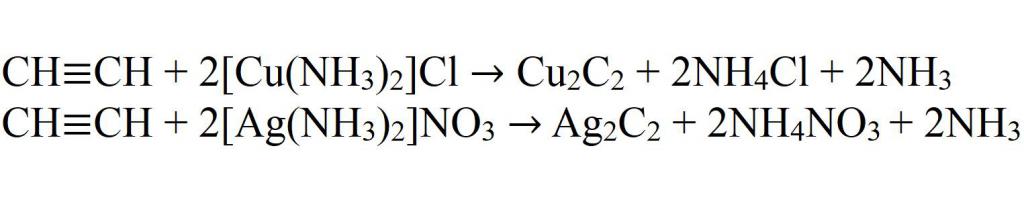
- Взаимодействие с амидом натрия.
- Димеризация. При этой реакции две молекулы ацетилена объединяются в одну. Необходим катализатор — соль одновалентной меди.
- Тримеризация. В этой реакции три молекулы ацетилена образуют бензол. Необходим нагрев до 70 °C, давление и катализатор.
- Тетрамеризация. В результате реакции получается восьмичленный цикл — циклооктатетраен. Для этой реакции также требуется небольшой нагрев, давление и соответствующий катализатор. Обычно это комплексные соединения двухвалентного никеля.
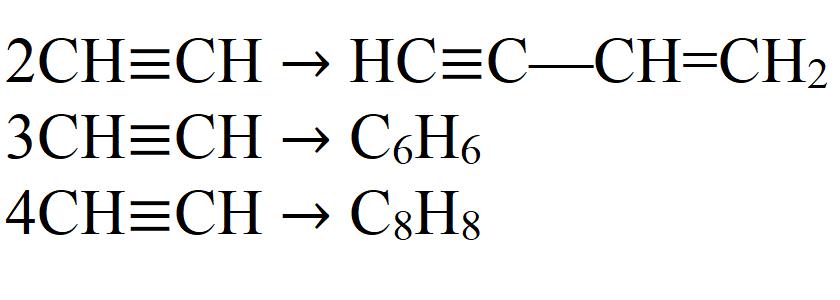
Это далеко не все химические свойства ацетилена.
В химически чистом виде ацетилен обладает слабым эфирным запахом. Технический ацетилен, благодаря наличию в нем примесей, в частности фосфористого водорода, имеет резкий специфический запах. Ацетилен легче воздуха. Газообразный ацетилен – бесцветный газ плотностью при 0 °С и 101,3 кПа (760 м рт. ст.) 1,173кг/м 3 . Молекулярная масса – 26,038.
Ацетилен способен растворяться во многих жидкостях. Его растворимость зависит от температуры: чем ниже температура жидкости, тем больше она способна «забрать» ацетилена. В практике производства растворенного ацетилена используют ацетон, который при температуре 15 °С растворяет до 23 объемов ацетилена.
Содержание фосфористого водорода в ацетилене должно быть строго ограничено, так как в момент образования ацетилена в присутствии воздуха при высокой температуре может произойти самовоспламенение.
Ацетилен — единственный широко используемый в промышленности газ, относящийся к числу немногих соединений, горение и взрыв которых возможны в отсутствии кислорода или других окислителей.
Еще в 1895 г. А.Л.Ле Шателье обнаружил, что ацетилен, сгорая в кислоте, дает очень горячее пламя (до 3150°С), поэтому его широко используют для сварки и резки тугоплавких металлов. Сегодня применение ацетилена для газопламенной обработки металлов испытывает сильную конкуренцию со стороны более доступных горючих газов (природный газ, пропан–бутан и т.д.). Однако преимущество ацетилена — в самой высокой температуре горения. В таком пламени очень быстро расплавляются даже толстые куски стали. Именно поэтому газопламенная обработка ответственных узлов машиностроительных конструкций производится только с помощью ацетилена, который обеспечивает наивысшую производительность и качество процесса сварки.
Кроме того, ацетилен широко используется в органическом синтезе разнообразных веществ — уксусного альдегида и уксусной кислоты, синтетических каучуков (изопренового и хлоропренового), поливинилхлорида и других полимеров.
Задание 13. Химические свойства и способы получения углеводородов. ЕГЭ 2021 по химии
Задача 1
Из предложенного перечня выберите две реакции, которые можно использовать для получения пентана.
- пентен-2 с водородом
- $C_5H_<11>Cl$ с Na
- $C_5H_<11>COONa$ с NaOH
- циклопентан с хлороводородом
- $C_5H_<11>Cl$ с KOH
Запишите в поле ответа номера выбранных реакций.
Решение
1) Водород присоединяется по месту разрыва π-связи.
3) Реакция Дюма, использующаяся для получения алканов.
Задача 2
Из предложенного перечня выберите две реакции, в каждой из которых образуется ацетилен.
- $CH_4 →↖<1500 °C>$
- $CH_4 →↖<1000 °C>$
- $CH_4 →↙↖<700 °C>$
- $CaC_2 + H_2O →$
- $CH_2=CH_2 + H_2 →↙↖$
Запишите в поле ответа номера выбранных реакций.
Решение
Ацетилен образуется при пиролизе метана при температуре 1500оС, а также в реакции карбида кальция с водой: $СаС_2 + Н_2О = НС≡СН + Са(ОН)_2$
Задача 3
Из предложенного перечня выберите два вещества, которые использовались для получения каучука, формула которого
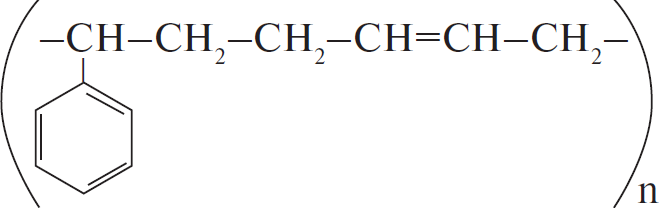
- винилхлорид
- дивинил
- изопрен
- стирол
- 2-хлорбутадиен-1,3
Запишите в поле ответа номера выбранных веществ.
Решение
Ищем самые схожие по строению вещества, а это дивинил, дающий цепочку из 4 атомов углерода и стирол, кольцо и еще два атома.
Задача 4
Из предложенного перечня выберите два ряда веществ, при взаимодействии каждого из которых с раствором перманганата калия будет наблюдаться изменение окраски раствора.
- ацетилен, п-ксилол, пропилен
- хлорэтан, пропан, бензол
- циклопентан, этилен, ацетилен
- этан, этилен, ацетилен
- пропилбензол, дивинил, пропин
Запишите в поле ответа номера выбранных рядов веществ.
Решение
Раствор перманганата калия $KMnO_4$ способен окислять спирты, альдегиды, непредельные углеводороды (алкены, алкины, диены) и их производные, боковые цепи ароматических углеводородов.
1) Ацетилен CH≡CH, пропилен $CH_3–CH=CH_2$ — непредельные углеводороды, должны обесцвечивать раствор перманганата калия; п-ксилол $C_6H_4(CH_3)_2$ окисляется раствором перманганата калия до терефталевой кислоты.
Вывод: все вещества удовлетворяют условию.
2) Хлорэтан $C_2H_5Cl$ — хлорпроизводное алкана, устойчив по отношению к раствору $KMnO_4$.
Вывод: не удовлетворяет условию задания.
3) Циклопентан $C_5H_<10>$ — циклический предельный углеводород, с раствором $KMnO_4$ не взаимодействует.
Вывод: не удовлетворяет условию задания.
4) Этан $C_2H_6$ — предельный углеводород, с раствором $KMnO_4$ не взаимодействует.
Вывод: не удовлетворяет условию задания.
5) Пропилбензол $C_6H_5CH_2CH_2CH_3$ — гомолог бензола, окисляется раствором $KMnO_4$ с образованием бензойной кислоты $C_6H_5COOH$.
1,3-Бутадиен (дивинил) — непредельный углеводород класса диенов, окисляется раствором $KMnO_4$. Пропин $CH≡C–CH_3$ — непредельный углеводород, окисляется раствором $KMnO_4$.
Вывод: все вещества удовлетворяют условию задания.
Задача 5
Из предложенного перечня выберите два вещества, которые могут реагировать с бромоводородом.
- метан
- полиэтилен
- бензол
- изобутилен
- циклопропан
Запишите в поле ответа номера выбранных веществ.
Решение
С бромоводородом могут реагировать вещества, в молекулах которых имеются кратные углерод-углеродные связи (C=C и C≡C), циклические углеводороды с напряжёнными циклами (циклопропан и циклобутан) и соли более слабых кислот.
1) Метан $CH_4$ — предельный углеводород, все связи одинарные, в реакции присоединения не вступает.
Вывод: ответ неверный.
2) Полиэтилен $(–CH_2–CH_2–)_n$ — высокомолекулярное вещество, в молекулах которого кратные связи отсутствуют.
Вывод: ответ неверный.
3) Бензол $C_6H_6$ — ароматический углеводород, в молекулах отсутствуют кратные связи, бромоводород присоединять не может.
Вывод: ответ неверный; ответы 4 и 5 — правильные («по остатку»).
Задача 6
Из предложенного перечня выберите два вещества, которые можно получить гидратацией алкина.
- бензол
- изопрен
- этаналь
- ацетон
- каучук
Запишите в поле ответа номера выбранных веществ.
Решение
При гидратации алкинов (в реакции Кучерова) из ацетилена образуется альдегид этаналь, а из алкинов с более длинной углеродной цепочкой — кетоны, так из пропина получается пропанон, также называемый ацетоном.
Задача 7
Из предложенного перечня выберите две реакции, которые можно использовать для получения пентана.
- пентен-2 с водородом
- $C_5H_<11>Cl$ с $Na$
- $C_5H_<11>COONa$ с $NaOH$
- циклопентан с хлороводородом
- $C_5H_<11>Cl$ с $KOH$
Запишите в поле ответа номера выбранных реакций.
Решение
1) При гидрировании пентена-2 образуется пентан.
2) Между хлорпентаном и натрием протекает реакция Вюрца — образуется декан.
3) Между натриевой солью карбоновой кислоты и гидроксидом натрия протекает реакция декарбоксилирования (реакция Дюма), продуктом которой является пентан.
4) При гидрогалогенировании циклопентана образуется хлорпентан.
5) В реакциях хлорпроизводных алканов с щелочами образуются алкены или спирты.
Таким образом, пентан образуется в реакции 1 и 3.
Задача 8
Из предложенного перечня выберите две реакции, в которые, в отличие от бутана, может вступать циклобутан.
- гидрирование
- горение
- этерификация
- гидрогалогенирование
- дегидрирование
Запишите в поле ответа номера выбранных реакций.
Решение
Циклобутан, в отличие от бутана, является циклическим углеводородом, а значит может подвергаться гидрированию, образуя бутан, а также гидрогалогенированию, получится 1-хлорбутан.
Задача 9
Из предложенного перечня выберите два вещества, которые могут преимущественно образовываться при действии спиртового и водного растворов гидроксида калия на 2-бромбутан.
- бутен-1
- бутен-2
- циклобутан
- бутиловый спирт
- бутанол-2
Запишите в поле ответа номера выбранных веществ.
Решение
Взаимодействие 2-бромбутана $CH_3-CHBr-CH_2-CH_3$ c водным раствором КОН атом брома меняется на гидроксильную группу — образуется бутанол-2 (реакция идёт по ионному механизму). Если используется спиртовой раствор, то реакция идёт по радикальному механизму, образуется бутен-2 (работает правило Зайцева).
Задача 10
Из предложенного перечня выберите два вещества, с которыми может взаимодействовать натрий.
- этилен
- этан
- хлорэтан
- ацетилен
- полиэтилен
Запишите в поле ответа номера выбранных веществ.
Решение
Натрий может реагировать с галогенпроизводными, а также с алкинами, у которых тройная связь находится у конца цепочки.
Задача 11
Из предложенного перечня выберите два ряда, каждое вещество которых взаимодействует с пропеном.
- $H_2, KOH, H_2O$
- $H_2O, H_2O_2, I_2$
- $H_2, O_2, CH_4$
- $HBr, NaMnO_4, Cl_2$
- $C_2H_6, H_2O, HBr$
Запишите в поле ответа номера выбранных рядов веществ.
Решение
Пропен $СН_3-СН=СН_2$ — алкен, вступает в реакции присоединения по двойной связи с галогенами, водородом, галогенводородами, водой. Проходят реакции замещения по sp3 гибридным атомам углерода (фрагмент СH3-) — с галогенами, также окисляется сильными окислителями, например перманганатом или пероксидом водорода. Под номером 2 даны вода, перекись водорода и йод, под номером 4 — бромоводород, перманганат натрия и хлор.
Задача 12
Из предложенного перечня выберите два типа реакций, в каждую из которых вступают как н-гептан, так и метилциклогексан.
- дегидрирование
- замещение атома водорода на гидроксогруппу
- присоединение галогеноводородов
- замещение с галогеноводородами
- риформинг
Запишите в поле ответа номера выбранных типов реакций.
Решение
Перед нами алкан и циклоалкан, они оба могут вступать в риформинг, потому что входят в состав нефти. Также все алканы и циклоалканы вступают в реакцию дегидрирования.
Задача 13
Из предложенного перечня выберите две реакции, которые можно использовать для получения соответственно циклобутана и циклопропана.
- дегидрирование бутана
- взаимодействие 1,4-дихлорбутана с цинком
- нагревание бутанола-1 с концентрированной H2SO4
- нагревание 1,4-дибромбутана и 1,3-дибромпропана со спиртовым раствором NaOH
- нагревание 1,3-дибромпропана с цинком
Запишите в поле ответа номера выбранных реакций.
Решение
Взаимодействие 1,4-дихлорбутана с цинком – метод получения циклоалканов дегалогенированием 1,4-дигалогенпроизводных. В данной реакции цинк присоединит к себе хлор, а углеродная цепь свернется в цкил, образовав циклобутан. Аналогичная реакция под номером 5 — нагревание 1,3-дибромпропана с цинком – является способом получения циклопропана.
Задача 14
Из предложенного перечня выберите два вещества, с каждым из которых реагирует аммиачный раствор оксида серебра.
- бутин-2
- бутен-2
- бутин-1
- бутен-1
- ацетилен
Запишите в поле ответа номера выбранных веществ.
Решение
Это реактив Толленса, он реагирует только с терминальными алкинами.
Задача 15
Из предложенного перечня выберите два вещества, которые преимущественно образуются при присоединении бромоводорода к метилпропену и 2-метилбутену-1 соответственно.
- 2-бром-2-метилпропан
- 1-бром-2-метилпропан
- 2-бром-2-метилбутан
- 1-бром-2-метилбутан
- 1,2-дибром-2-метилбутан
Запишите в поле ответа номера выбранных веществ.
Решение
При присоединении бромоводорода к метилпропену $(СН_3)_2С=СН_2$, по правилу Марковникова, водород присоединяется к наиболее гидрированному атому углерода — крайнему, а бром — к центральному. Продукт реакции — 2-бром-2-метилпропан.
При присоединении бромоводорода к 2-метилбутену-1 $CH_2=C(CH_3)-CH_2-CH_3$ действует то же правило, водород присоединяется к первому углероду, так как с ним соединено больше водорода, а бром — ко второму. Получается 2-бром-2-метилбутан.